Etylen glicol được biết đến là hợp chất đóng vai trò vô cùng quan trọng trong đời sống, nghiên cứu. Vậy Etylen glicol là gì? Tính chất nổi bật của Etylen glicol là gì? Etilen được dùng trong những lĩnh vực nào? Để hiểu rõ hơn, chúng ta cùng tìm hiểu chi tiết trong nội dung bài viết dưới đây nhé!

Etylen glicol là gì?
Etylen glicol là một hợp chất hữu cơ có tính chất không màu, không mùi, chất lỏng dạng siro và có hương vị ngọt.
Công thức Etylen glicol là (CH2OH)2 hay C2H6O2.
Etylen glicol tồn tại trong không khí dạng hơi và được sử dụng để làm chất chống ăn mòn và nguyên liệu thô sản xuất sợi polyester.
Tính chất nổi bật của Etylen glicol là gì?
Etylen glicol có tính chất nổi bật như sau.
Tính chất vật lý
- Là chất dễ bay hơi, không màu, không mùi, tan trong nước và hầu hết các dung môi hữu cơ khác.
- Khối lượng riêng: 1,1132 g/cm3.
- Điểm nóng chảy: −12,9°C (260,2 K; 8,8°F).
- Điểm sôi: 197,3°C (470,4 K; 387,1°F).
- Áp suất hơi: 0,06 mmHg (20°C).
- Độ nhớt 1,61 × 10−2 N*s/m2.
Tính chất hóa học
Công thức Etylen glicol là (CH2OH)2 hay C2H6O2. Nhìn vào công thức này có thể thấy rằng chất có chứa 2 nhóm -OH. Vì thế nen chúng có những tính chất của một ancol cơ bản như sau.
- Phản ứng với kim loại: C2H4O2 + 2Na → C2H2O2Na2 + H2
- Phản ứng với Đồng(II) oxit: Phản ứng này dùng để nhận biết Etylen glicol và các chất nhiều hơn một nhóm -OH (poliancol).
- Phản ứng este hóa: C2H4(OH)2 + 2HCOOH → 2H2O + C2H4(OOCH)2
- Phản ứng tách nước: Phản ứng này tuân thủ theo quy tắc Zai-xép: Nhóm –OH ưu tiên tách cùng với H ở bậc cacbon cao hơn bên cạnh để tạo thành liên kết đôi C=C mang nhiều nhóm ankyl hơn.
- Phản ứng oxi hóa: HOCH2CH2OH + O2 → (CHO)2 + 2H2
Cu(OH)2 + HOCH2CH2OH + O2 → OHCH2 – CH2O – Cu – OH2C – CH2OH + 2H2O.
Cách sản xuất Etylen glicol
Etylen glicol được sản xuất theo 2 cách sau.

Cách 1: Etilen được sản xuất từ ethylene
Etilen được sản xuất từ ethylene, thông qua ethylene oxide trung gian. Ethylene oxit phản ứng với nước để tạo ra ethylene glycol theo phương trình hóa học dưới sự xúc tác của 2 axit hoặc bazơ hoặc có thể xảy ra ở pH trung tính ở nhiệt độ cao.
C2H4O + H2O → HO – CH2CH2 – OH
Cách 2: Etylen glicol được sản xuất từ carbon monoxide
Etylen glicol được sản xuất từ carbon monoxide ở các nước có trữ lượng than lớn, có tiềm năng về hóa học khí tổng hợp bao gồm Trung Quốc. Sự oxy hóa cacbonyl hóa metanol với đimetyl oxalat cung cấp một cách tiếp cận đầy hứa hẹn cho việc sản xuất etylen glycol dưới dạng C1 ethylene glycol. Dimethyl oxalat có thể được chuyển đổi thành ethylene glycol với năng suất cao (94,7%) bằng cách hydro hóa với chất xúc tác đồng.
Ứng dụng của etilen
Etylen glicol (etilen) được ứng dụng trong nhiều mục đích khác nhau như.

- Etylen glicol được dùng để làm dung môi mà chủ yếu nhất là công thức chống đông chiếm 50%, nguyên liệu thô sản xuất polyester như polyethylene terephthalate (PET) chiếm 40%.
- Là phương tiện vô cùng hữu hiệu dùng để làm chất làm lạnh và chất chuyển nhiệt
- Etylen glicol được dùng để truyền nhiệt đối lưu và máy làm mát bằng chất lỏng trong lĩnh vực ô tô.
- Etilen được dùng trong các hệ thống điều hòa không khí lạnh hoặc hệ thống phải làm mát dưới nhiệt độ đông của nước.
- Etylen glicol là chất lỏng vận chuyển nhiệt thông qua sử dụng máy bơm nhiệt địa nhiệt trong hệ thống sưởi ấm, làm lạnh địa nhiệt.
- Etylen glicol dùng làm chất chống đông.
- Ethylene glycol nguyên chất đóng băng ở khoảng -12 ° C (10.4 ° F), nhưng khi trộn với nước, hỗn hợp không dễ kết tinh, và do đó điểm đóng băng của hỗn hợp không còn hoạt động.
- Nhờ có khả năng ăn mòn, Etylen glicol trở thành hỗn hợp đông lạnh (chống ăn mòn) để bảo quản các mô và mô sinh học ở nhiệt độ thấp.
- Dùng làm chất khử nước: Etylen glicol được sử dụng trong ngành công nghiệp khí đốt tự nhiên để loại bỏ hơi nước từ khí tự nhiên trước khi gia công thêm theo cùng một cách như triethylene glycol (TEG).
- Dùng làm chất làm khô: Etylen glicol được sử dụng rộng rãi để ức chế sự hình thành clathrates khí tự nhiên trong các ống dẫn đa dải dài truyền khí tự nhiên từ các cánh đồng khí từ xa đến cơ sở chế biến khí.
Etylen glicol có độc không?
Etylen glicol có độ độc hại vừa phải, nguy hiểm lớn do vị ngọt của nó, có thể thu hút trẻ em và động vật. Khi ăn phải, etilen bị oxy hóa thành axit glycolic, và chuyển hóa thành axit oxalic, độc tố.
Theo chẩn đoán, có thể bị nghi ngờ khi nhìn thấy tinh thể canxi oxalat trong nước tiểu, khi nhiễm toan hoặc tăng khoảng cách osmol trong máu. Chẩn đoán được xác nhận bằng cách đo nồng độ etylen glicol trong máu. Tuy nhiên, nhiều bệnh viện không có khả năng thực hiện xét nghiệm này.
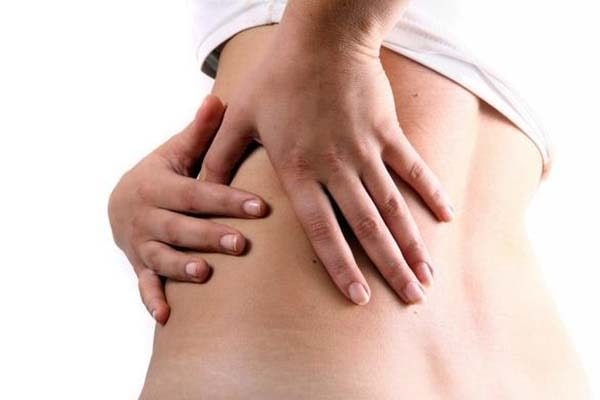
Ethylene glycol ảnh hưởng đến sức khỏe con người như thế nào?

Nếu tiếp xúc etylen glicol với một lượng thấp sẽ gây buồn nôn, ói mửa, có máu hoặc không có nước tiểu, thở nhanh, hạ thân nhiệt, hoa mắt, huyết áp thấp hoặc cao, nhịp tim nhanh, nói lắp, bị kích thích da, mắt, mũi và họng.
Các triệu chứng ngộ độc etylen glicol gồm 2 giai đoạn:
- Triệu chứng sớm sẽ bị nôn mửa và đau bụng.
- Triệu chứng sau này làm giảm mức độ ý thức, đau đầu và co giật. Để lâu sẽ bị suy thận và tổn thương não. Nghiêm trọng hơn có thể gây tử vong nếu sau khi uống dù chỉ một lượng nhỏ.
Cách điều trị nếu bị nhiễm độc ethylene glycol
Khi uống phải Etylen glicol nếu phát hiện sớm và điều trị lập tức thì có thể cứu chữa kịp thời. Cách điều trị là dùng thuốc giải độc.
Thuốc giải độc được ưu tiên là fomepizole với ethanol được sử dụng nếu không có sẵn. Thẩm tách máu có thể được sử dụng ở những nơi tổn thương nội tạng hoặc mức độ nhiễm toan cao.
Ngoài ra, khi bị nhiễm độc chất etylen glicol có thể điều trị bằn phương pháp khác như: natri bicarbonat, thiamine và magiê.